science
Les principaux systèmes d’édition de gènes de nouvelle génération élargissent les applications cliniques et de recherche de la technologie
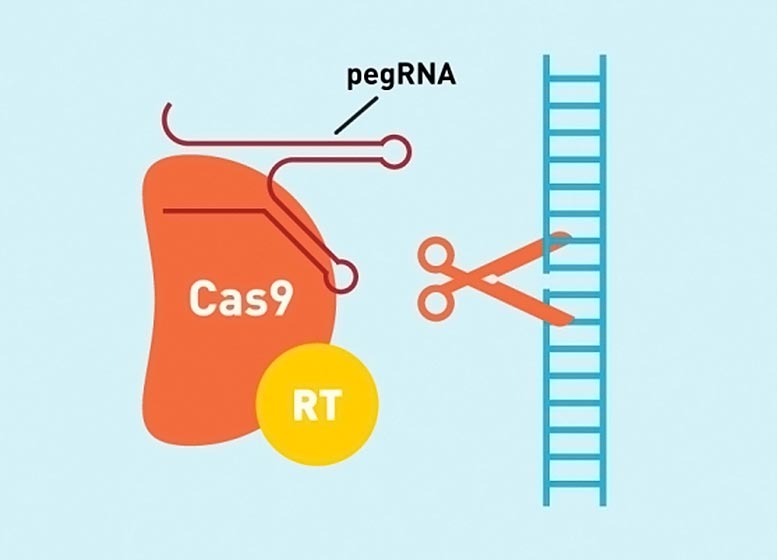
Les chercheurs ont amélioré l’efficacité de l’édition primaire, une technologie d’édition de gènes polyvalente basée sur CRISPR, et ont utilisé le système amélioré pour corriger les mutations pathologiques dans les cellules.
Les scientifiques ont développé un ensemble d’outils moléculaires qui augmentent l’efficacité d’une technologie d’édition de gènes appelée édition primaire pour une variété de types de cellules et de gènes cibles, élargissant ainsi les applications thérapeutiques et de recherche de la technologie. Dans deux nouvelles études, les chercheurs ont utilisé des systèmes d’édition primaires améliorés pour corriger les mutations associées à plusieurs maladies neurodégénératives, métaboliques et cardiovasculaires.
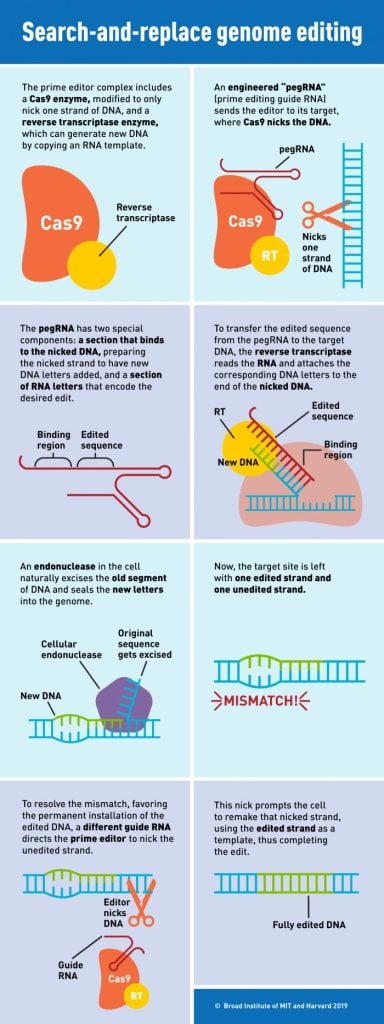
Il a été décrit pour la première fois dans 2019L’édition primaire est une méthode précise d’édition de gènes qui a le potentiel de corriger la grande majorité des variations génétiques connues à l’origine de maladies. Les chercheurs peuvent utiliser l’édition initiale pour travailler ADN Substitutions, insertions et suppressions sur des sites cibles dans des cellules humaines et animales. Cependant, l’efficacité de l’édition varie en fonction du type de cellule en cours d’édition et du site cible dans le génome.
Pour développer davantage la technologie, les scientifiques du Broad Institute avec Et Harvard est une amélioration par rapport à un élément clé du système d’édition de base appelé ARN guidé par l’édition ou « pegRNA », qui codent la modification prévue et dirigent la machine d’édition initiale. Dans une étude publiée récemment dans biotechnologie naturelle, les chercheurs ont montré que les pegRNAs peuvent être dégradés dans les cellules, coupant les pegRNAs qui interfèrent avec l’édition initiale. Ils ont développé de nouveaux pegRNA qui sont protégés de la dégradation dans les cellules, ce qui a augmenté l’efficacité de l’édition à grande échelle.
Dans une deuxième étude publiée récemment dans celluleChercheurs extensifs, collaborant avec des scientifiques de université de Princeton et l’Université de Californie à San Francisco (UCSF), ont identifié les voies cellulaires qui limitent l’efficacité de l’édition primaire et ont utilisé ces informations pour développer la prochaine génération de systèmes d’édition primaire.
Dans les deux études, les chercheurs ont montré que les nouveaux systèmes pourraient modifier plus efficacement les mutations associées La maladie d’Alzheimer Maladie cardiaque, drépanocytose, maladie à prions, diabète de type 2 et autres maladies, avec moins de sous-produits indésirables produits.
David Liu, auteur principal des deux études, a déclaré le professeur Richard Merkin et directeur du Merkin Institute for Transformative Technologies in Health Care au Broad Institute, professeur à l’Université Harvard et chercheur au Howard Hughes Medical Institute.
Guide d’ingénierie plus stable
L’édition initiale permet aux scientifiques de corriger la grande majorité des mutations pathogènes connues – y compris les substitutions, les insertions ou les suppressions de plusieurs dizaines de paires de bases – à des emplacements spécifiques du génome. Contrairement à d’autres techniques d’édition du génome, l’édition primaire n’implique pas de couper les deux brins d’ADN et, par conséquent, réduit les risques de résultats d’édition indésirables ou de réponses cellulaires indésirables. (Voir le tableau ci-dessus pour plus d’informations sur le fonctionnement de l’édition principale.) Des centaines de groupes de recherche utilisent maintenant l’édition principale pour étudier et corriger les mutations dans une grande variété d’organismes, notamment le riz, le blé, le poisson zèbre et les souris.
Après avoir décrit le montage initial pour la première fois en 2019, l’équipe de Liu a continué à développer la technologie. dans le biotechnologie naturelle Dans l’étude, ils ont découvert une vulnérabilité dans les pegRNAs qui réduit l’efficacité. Ils ont découvert que la longue chaîne de ARN A l’extrémité du pegRNA qui code la modification était soumis à une dégradation par les enzymes cellulaires. Les pegRNA dégradés ne peuvent pas arbitrer l’édition initiale et également « empoisonner » le système d’édition principal en bloquant l’accès aux sites cibles par les pegRNA intacts.
Ensuite, les chercheurs ont recherché les structures protectrices qu’ils pourraient ajouter aux pegRNA. Ils ont testé plusieurs séquences d’ARN différentes, identifiant celles qui se replient dans des structures en forme de nœud qui les protègent des enzymes dégradant l’ARN. Lorsqu’ils ont modifié les pegRNA pour inclure des nœuds et des séquences de contact, ils ont observé une augmentation significative de l’efficacité d’édition initiale, indiquant que les nouvelles structures préservaient la matrice d’ARN pour l’édition.
En utilisant des pegRNA modifiés, ou epegRNA, dans un groupe de lignées cellulaires de mammifères, les chercheurs ont constaté que les epegRNA augmentaient l’efficacité d’édition initiale de trois à quatre en moyenne, avec de plus grandes améliorations dans les lignées cellulaires dans lesquelles l’édition initiale était auparavant plus difficile.
Orientation de la cellule vers les éditions initiales
dans le cellule Dans l’étude, l’équipe et les collaborateurs de Liu ont conçu le composant protéique du système d’édition primaire pour augmenter l’efficacité et réduire les sous-produits produits dans un large éventail de types de cellules, y compris les cellules de patients.
Les chercheurs visent à mieux comprendre les facteurs cellulaires qui déterminent les résultats initiaux de l’édition afin de pouvoir concevoir des systèmes plus efficaces. L’équipe soupçonnait que certaines protéines cellulaires actives au cours d’une partie clé du processus d’édition primaire – lorsque la cellule répare les molécules d’ADN créées par les principaux éditeurs – pourraient entraver ou même inverser la modification et augmenter la production de sous-produits indésirables. Pour tester cette hypothèse, les chercheurs ont collaboré avec des équipes dirigées par Brett Adamson, professeur adjoint à l’Université de Princeton. et Jonathan Wiseman, professeur à l’UCSF au début de l’étude, et maintenant professeur au MIT et membre du Whitehead Institute et chercheur au Howard Hughes Medical Institute. À l’aide d’écrans CRISPR basés sur les interférences, les équipes ont systématiquement examiné l’effet de la désactivation de chacun des 476 gènes de réparation de l’ADN différents lors de l’édition initiale.
Sur la base de ces résultats, les chercheurs se sont concentrés sur un processus appelé réparation des mésappariements, qui se produit naturellement dans les cellules pour corriger les mésappariements de l’ADN produits lors de la réplication et de la réparation de l’ADN. Ils constatent que la réparation des non-concordances interfère avec l’édition initiale, réduit l’efficacité de l’édition et augmente la proportion d’insertions ou de suppressions involontaires.
Forte de cette idée, l’équipe a développé de nouveaux systèmes d’édition primaires, qu’ils ont nommés PE4 et PE5, qui incluent une protéine, MLH1dn, que les chercheurs ont conçue pour bloquer temporairement un composant de réparation des mésappariements. Dans les cellules où se produit la réparation des mésappariements, les chercheurs ont découvert que PE4 et PE5 augmentaient considérablement l’efficacité de l’édition et produisaient beaucoup moins de sous-produits par rapport aux systèmes d’édition primaires actuels.
Enfin, les scientifiques ont créé PEmax, qui a amélioré l’architecture et l’amino aigre Séquence de machines de montage primaires. La combinaison des améliorations des systèmes PE4, PE5, PEmax et epegRNAs a entraîné une augmentation de 10 à 100 fois de l’efficacité d’édition par rapport aux systèmes actuels.
« En rassemblant l’expertise de différents groupes de recherche, nous avons pu apprendre comment l’édition initiale fonctionnait et améliorer certaines parties du système », a déclaré Adamson. « Cette étude est un bel exemple de la façon dont la compréhension de base peut conduire la conception expérimentale. »
vers la guérison
Dans de nombreux cas, les améliorations combinées des epegRNAs et du PE4/5/max permettent aux scientifiques de créer plus facilement des modèles cellulaires de la maladie, dit Liu, une étape critique vers le développement de traitements.
L’équipe utilise maintenant ces systèmes pour traiter des modèles cellulaires et animaux de maladies génétiques, et continuera d’explorer la biologie fondamentale de ces systèmes.
« Toutes ces innovations sont synergiques », a déclaré Liu. « Grâce à ces améliorations, nous avons pu modifier efficacement et proprement des types cellulaires importants qui pourraient un jour aider les patients atteints de maladies à composante génétique. Ces résultats suggèrent également qu’il existe d’autres stratégies qui peuvent encore améliorer l’édition initiale. »
Les références:
« Systèmes d’édition primaires améliorés en manipulant des déterminants cellulaires pour modifier les résultats » par Peter J. Chen, Jeffrey A. Hausmann, John Yan, Frederic Nipping, Purnima Ravizankar, Ben Fang Chen, Sidi Chen, James W. Nelson, Gregory A. , Mostafa Şahin, Mark J. Osborne, Jonathan S. Weissman, Brett Adamson et David R. Leo, 14 octobre 2021, cellule.
DOI : 10.1016 / j.cell.2021.09.018
« Les pegRNA conçus améliorent l’efficacité de l’édition initiale » par James W. Nelson, Peyton B. Randolph, Simon B. Sheen, Kelsey A. Everett, Peter J. Chen, Andrew F. Chen, Alvin Hsu et David R. Liu, 4 octobre 2021, disponible ici. biotechnologie naturelle.
DOI : 10.1038 / s41587-021-01039-7
Ce travail a été soutenu par le Merkin Institute for Transformative Technologies in Health Care, les National Institutes of Health, le Howard Hughes Medical Institute, la Fondation Loulou et la Fondation Bill & Melinda Gates.

« Spécialiste de la télévision sans vergogne. Pionnier des zombies inconditionnels. Résolveur de problèmes d’une humilité exaspérante. »
science
Le chef de l’Agence spatiale américaine veut parler avec la Chine des débris spatiaux

29 août 2024
Le chef du commandement spatial américain espère que la prochaine fois que la Chine lancera un missile laissant derrière elle des débris spatiaux de longue durée, Pékin avertira Washington à l’avance, plutôt que de laisser les États-Unis découvrir par eux-mêmes le chaos orbital.
Parlez dans L’efficacité du Mitchell Institute for Aerospace Studies Lors d’une réunion à la base spatiale Peterson, au Colorado, le 28 août, le général Stephen N. Whiting a souligné deux incidents récents impliquant des débris spatiaux chinois comme étant une source de préoccupation et la nécessité d’améliorer la communication à l’avenir.
« Nous venons de voir le lancement de leur version de Constellation du soleil « Cela a laissé plus de 300 débris en orbite – une fusée Longue Marche 6A », a déclaré Whiting. « Il y a moins de deux ans, ils avaient une autre fusée, qui a mis plus de 500 débris à longue durée de vie… J’espère que la prochaine fois. que « Dans un missile comme celui-ci, il laisse beaucoup de débris. Ce ne sont pas nos capteurs qui détectent cela en premier, mais nous obtenons des communications qui nous aident à comprendre cela, tout comme nous communiquons avec les autres. »
L’incident le plus récent impliquant une fusée Longue Marche 6A s’est produit au début du mois, lorsque le lanceur transportait les 18 premiers satellites d’une constellation de communications prévue pour rivaliser avec Starlink. La fusée s’est brisée en orbite terrestre basse (LEO) quelques jours plus tard, répandant des débris et suscitant des inquiétudes parmi les experts. La société privée de suivi spatial a rapporté que la désintégration pourrait produire plus de 10… 900 épaves shrapnel.
Whiting a noté que les débris provenaient de l’étage supérieur de la fusée après le lancement des satellites, indiquant que la mission était « généralement réussie ». Cependant, à des altitudes plus élevées, les débris resteront en orbite plus longtemps.
« Nous ne voulons certainement pas voir ce genre de débris », a ajouté Whiting.
Les débris se trouvent généralement sur des orbites inférieures à 600 km (373 miles). Il revient sur Terre après quelques annéesÀ une altitude de 800 km, sa décomposition peut prendre des siècles. Avec de plus en plus de satellites en orbite terrestre basse et des débris persistants provenant de lancements peu judicieux, La probabilité de collisions continue d’augmenter.
Selon le général à la retraite Kevin Shelton, directeur du Centre d’excellence sur l’énergie spatiale du Mitchell Institute, les États-Unis ont déjà eu des problèmes similaires avec des débris à haute altitude, mais ont commencé à évacuer le carburant et les gaz des étages de fusée avant d’entrer en orbite. Cette pratique réduisait les débris et le risque de désintégration, et la Russie l’adopta peu après. Whiting a déclaré qu’on ne savait pas actuellement si la Chine utilisait cette méthode.
« Depuis des décennies, les États-Unis s’intéressent tellement à l’espace que nous avons mis la grande majorité de nos données de suivi à la disposition du monde entier », a déclaré Whiting. « Chaque jour, nous analysons tous les satellites actifs à la recherche de tous ces débris, et nous en informons tout le monde, y compris les Chinois et les Russes… parce que nous ne voulons pas que les satellites heurtent des débris et laissent derrière eux d’autres débris. »
Le développement rapide des capacités spatiales et l’augmentation significative des déploiements de satellites par la Chine et la Russie restent une préoccupation majeure quant à la manière dont les États-Unis abordent le domaine spatial. Chef adjoint des opérations spatiales, le général Michael A. Gotlin a souligné que les récentes mesures prises par ces pays prouvent leur intention d’opérer de manière dangereuse dans ce domaine.
« Ils créent beaucoup de débris et d’orbites que nous devons contourner, ou ils mettent en danger des choses comme la Station spatiale internationale », a déclaré Gotlin lors du Sommet AFCEA/INSA sur le renseignement et la sécurité nationale à Rockville, Maryland, le 28 août. Il a ajouté : « Ils ne se soucient même pas de la sécurité des astronautes. Si ce n’est pas dangereux et non professionnel, je ne sais pas ce que c’est. »
En novembre 2021, la Russie a procédé à un test de missile antisatellite, aboutissant à la création d’un Grande quantité de débris En orbite terrestre basse, ce qui présente un danger pour la Station spatiale internationale et incite l’équipage à prendre des mesures de précaution. En outre, Moscou a également été témoin Une série de fuites de liquide de refroidissement Ces dernières années, la Chine a lancé son propre vaisseau spatial. Même s’il n’y a pas de négociations prévues avec la Russie sur le développement spatial, les espoirs sont grands d’une communication plus active avec Pékin sur les alertes spatiales.
« Nous donnons ces avis aux Chinois, et au cours de l’année dernière, nous avons vu à plusieurs reprises qu’ils nous ont donné quelques avis en retour, et je pense que c’est une chose positive. Nous n’avons aucune discussion. prévu avec la Russie », a déclaré Whiting.

« Spécialiste de la télévision sans vergogne. Pionnier des zombies inconditionnels. Résolveur de problèmes d’une humilité exaspérante. »
science
À la recherche de pierres précieuses : caractérisation de six planètes géantes en orbite autour de naines froides
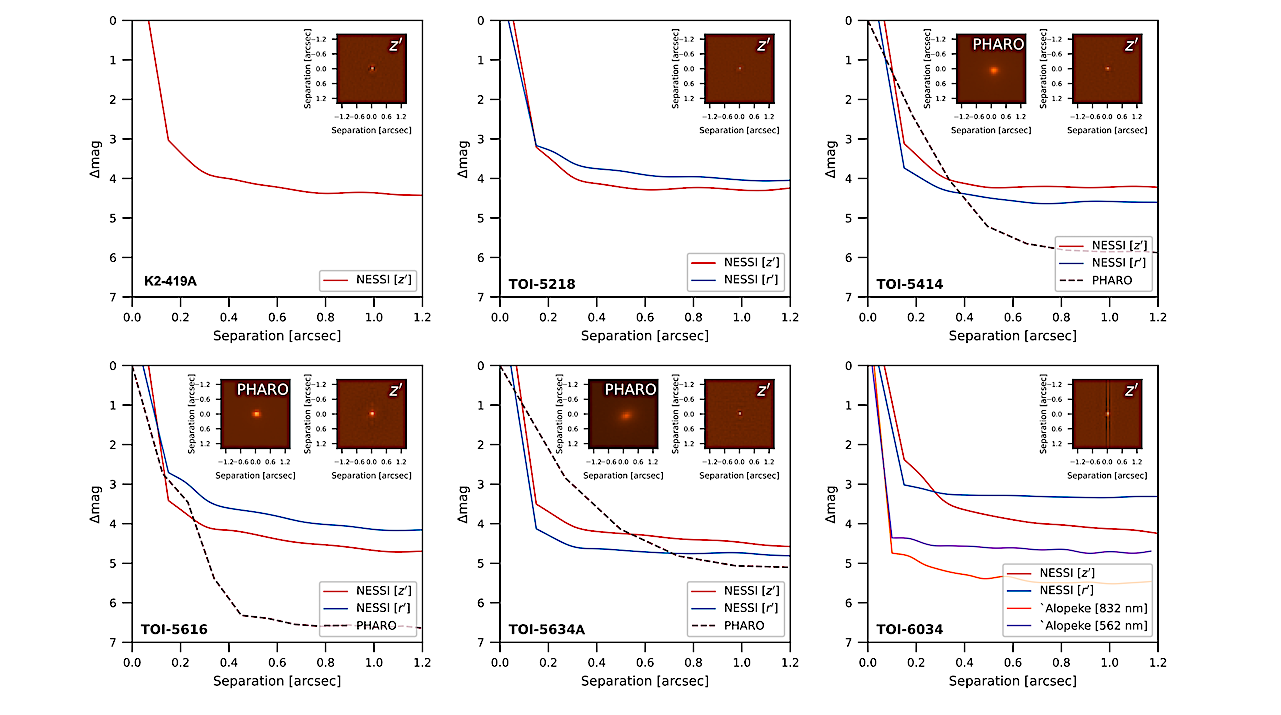
Données d’imagerie à contraste élevé pour toutes les cibles. Dans chaque panneau, nous montrons la limite de contraste de 5σ atteinte en fonction de la séparation angulaire de l’étoile hôte pour chaque ensemble de données à contraste élevé. Nous traçons également des cachets postaux de 1,4″ × 1,4″ d’images NESSI reconstruites en bande z (encadré à droite dans chaque panneau) pour toutes les cibles et des images AO (encarts à gauche) pour TOI-5414, TOI-5616, TOI-5634A et TOI-6034. — astro-ph.EP
Les exoplanètes géantes transitant autour d’étoiles naines de type M (GEMS) sont rares, en raison de la faible masse de leurs étoiles hôtes. Cependant, la couverture de l’ensemble du ciel par TESS a permis d’en détecter un nombre croissant pour permettre des enquêtes statistiques telles que le GEMS Search Survey.
Dans le cadre de cet effort, nous décrivons les observations de six planètes géantes en transit, qui incluent des mesures de masse précises pour deux GEMS (K2-419Ab, TOI-6034b) et une validation statistique de quatre systèmes, qui incluent une vérification et des limites de masse supérieures pour trois d’entre elles. (TOI-5218b, TOI-6034b). 5616b, TOI-5634Ab), tandis que le quatrième système – TOI-5414b – est classé comme « planète potentielle ».
Nos observations incluent les vitesses radiales du Habitable Zone Planet Finder sur le télescope Hobby-Eberly et de l’observatoire Maroon-X sur Gemini-North, ainsi que la photométrie et l’imagerie à contraste élevé provenant de plusieurs installations au sol. En plus de la photométrie TESS, K2-419Ab a également été observé et validé statistiquement dans le cadre de la mission K2 au cours des campagnes 5 et 18, qui fournit des contraintes orbitales et planétaires précises malgré la faible luminosité de l’étoile hôte et la longue période orbitale d’environ 20,4 jours.
Avec une température d’équilibre de seulement 380 K, K2-419Ab est l’une des planètes en transit les plus froides et les mieux caractérisées connues. TOI-6034 a un compagnon tardif de type F à environ 40 secondes d’arc, ce qui en fait la première étoile hôte GEMS à avoir un ancien compagnon binaire sur la séquence principale. Ces confirmations s’ajoutent au petit échantillon existant de planètes en transit GEMS confirmées.
Shubham Kanodia, Arvind F. Gupta, Caleb I. Canas, Lea Marta Bernabo, Varghese Reggie, T. Hahn, Madison Brady, Andreas Seyfart, William D. Cochrane, Nydia Morrell, Ritvik Basant, Jacob Bean et Chad F. Bender, Zoé L. De Bors, Alison Perella, Alexina Birkholz, Nina Brown, Franklin Chapman, David R. Ciardi, Catherine A. Clark, Ethan J. Cotter, Scott A. Diddams, Samuel Halverson, Susan Hawley, Leslie Hebb, Ray Holcomb, Steve B. Howell, Henry A. Kobolnicki, Adam F. Kowalski, Alexander Larsen, Jessica Libby Roberts, Andrea S. J. Lin, Michael B. Lund, Raphael Locke, Andrew Munson, Joe B. Ninan, Brooke A. Parker, Nishka Patel, Michael Rudrak, Gabrielle Ross, Arpita Roy, Christian Schwab, Jomundur Stefansson, Aubrey Thoms, Andrew Vanderberg
Commentaires : Accepté dans AJ
Sujets : Astrophysique terrestre et planétaire (astro-ph.EP)
Citer ce qui suit : arXiv:2408.14694 [astro-ph.EP] (ou arXiv :2408.14694v1 [astro-ph.EP] (pour cette version)
https://doi.org/10.48550/arXiv.2408.14694
Concentrez-vous pour en savoir plus
Date de publication
De : Shubham Kanodia
[v1] Lundi 26 août 2024, 23:47:24 UTC (5 169 Ko)
https://arxiv.org/abs/2408.14694
Astrobiologie

« Spécialiste de la télévision sans vergogne. Pionnier des zombies inconditionnels. Résolveur de problèmes d’une humilité exaspérante. »
science
La Federal Aviation Administration des États-Unis a immobilisé les fusées Falcon 9 de SpaceX dans l’attente d’une enquête sur un rare accident d’atterrissage au large des côtes.

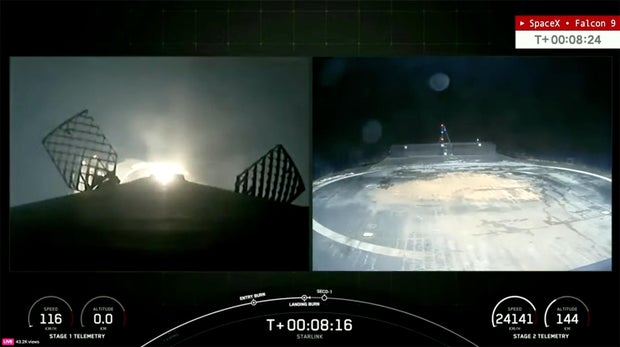
La Federal Aviation Administration a immobilisé les fusées Falcon 9 de SpaceX en attendant une enquête visant à déterminer pourquoi le propulseur du premier étage s’est arrêté. Collision avec un bateau de débarquement tôt mercredi après avoir contribué au lancement d’un autre lot de satellites Internet Starlink.
après Se lever Après avoir reporté mardi soir le lancement du vaisseau spatial avec équipage Polaris Dawn en raison de prévisions météorologiques à long terme défavorables, SpaceX a continué à travailler sur le premier des lancements consécutifs de satellites Starlink, un depuis la Floride et un depuis la Californie.
Mais le deuxième vol a été annulé après que le premier étage utilisé lors du lancement en Floride s’est brisé et est tombé dans l’océan Atlantique alors qu’il tentait d’atterrir sur un drone SpaceX stationné à des centaines de kilomètres au nord-est de Cap Canaveral.
EspaceX
La FAA a déclaré qu’elle ordonnerait une enquête, immobilisant efficacement les fusées Falcon 9 de SpaceX – y compris la fusée Polaris Dawn – jusqu’à ce que l’enquête soit terminée et que les mesures correctives soient approuvées.
« Le retour en vol de la fusée Falcon 9 dépend de la détermination par la FAA que tout système, processus ou procédure lié à l’anomalie n’a pas d’impact sur la sécurité publique », a déclaré la FAA dans un communiqué.
« En outre, SpaceX devra peut-être demander et obtenir l’approbation de la FAA pour modifier sa licence qui inclut des actions correctives et satisfaire à toutes les autres exigences de licence », a ajouté l’agence.
Mardi soir, SpaceX a reporté un lancement prévu mercredi Mission Aube PolarisLe lancement d’un vol commercial comprenant la première sortie dans l’espace par une organisation non gouvernementale a été reporté à vendredi au plus tôt en raison des conditions météorologiques attendues à la fin de la mission. Le lancement a été suspendu indéfiniment dans l’attente d’une enquête sur l’accident à l’atterrissage.
L’échec de l’atterrissage a mis fin à une séquence de 267 récupérations consécutives réussies de boosters remontant à février 2021. Cependant, le deuxième étage de la fusée Falcon 9 a réussi à transporter 21 satellites Starlink sur leur orbite prévue.
L’atterrissage du premier étage semblait normal jusqu’au moment de l’atterrissage, lorsque plus de flammes que d’habitude sont apparues autour de la base de la fusée à l’approche du pont de la fusée. L’une des jambes d’atterrissage s’est effondrée immédiatement après l’atterrissage et la fusée d’appoint, masquée par le feu et la fumée, s’est renversée par-dessus le côté de la péniche de débarquement dans l’océan Atlantique.
EspaceX
EspaceX
EspaceX
« Après une ascension réussie, le premier étage d’une fusée Falcon 9 s’est retourné après son atterrissage sur le vaisseau spatial sans pilote ‘Zero Gravity' », SpaceX Il a dit sur les réseaux sociaux« Les équipes évaluent les données de vol et l’état du missile. »
Il s’agissait du 23e premier étage de la fusée B1062, qui s’est avéré être son dernier lancement et atterrissage, un nouveau record de réutilisabilité. SpaceX autorise les premiers étages de la fusée Falcon 9 pour un maximum de 40 vols par étage.
Peu de temps après le déploiement des satellites Starlink en Floride, la société a annulé le lancement en Californie, qui était prévu à 5 h 58 HAE, pour donner aux ingénieurs plus de temps pour examiner la télémétrie et les séquences vidéo, à la recherche de tout signe de problème. affecter d’autres missiles.
« Retrait de notre deuxième lancement @Starlink la nuit pour donner à l’équipe le temps d’examiner les données d’atterrissage du booster du lancement précédent », a déclaré SpaceX. Il a dit« Une nouvelle date de lancement cible sera partagée une fois disponible. »

« Spécialiste de la télévision sans vergogne. Pionnier des zombies inconditionnels. Résolveur de problèmes d’une humilité exaspérante. »
-
entertainment2 ans ago
Découvrez les tendances homme de l’été 2022
-
Top News2 ans ago
Festival international du film de Melbourne 2022
-
Tech1 an ago
Voici comment Microsoft espère injecter ChatGPT dans toutes vos applications et bots via Azure • The Register
-
science3 ans ago
Écoutez le « son » d’un vaisseau spatial survolant Vénus
-
science2 ans ago
Les météorites qui composent la Terre se sont peut-être formées dans le système solaire externe
-
Tech2 ans ago
F-Zero X arrive sur Nintendo Switch Online avec le multijoueur en ligne • Eurogamer.net
-
Top News2 ans ago
Comment parier sur le basket : tous les conseils pour continuer et s’amuser
-
entertainment1 an ago
Seven révèle son premier aperçu du 1% Club